Sorhocam.com 2014 yılında Ziraat Mühendisi Arafa KARAÇELEBİ tarafından kurulmuş olup herkesin faydalanabilmesi için ücretsiz olarak hizmet vermektedir.
Azot Tayini Nedir?
Sembolü N, atom numarası 7, Latince’si Nitrogenium, İngilizce’si Nitrogen, Fransızca’sı Azote, Almanca’sı Stickstoff olan azotun atom tartısı 14.008, değerliği ise - 3 , + 1 , + 2 , + 3 , + 4 , + 5 dir. Azot tabiatta NaNO3, yani Şili Güherçilesi ve guano (Bazı organik azot bileşikleri karışımı) şeklinde bulunur. Her ikisi de organik cisimlerden teşekkül etmişlerdir. Azotun elementel halde bulunduğu yer havadır, azot havanın arz yüzeyine yakın olan yerlerinde hac men % 78,09 oranında bulunur.
Kimyasal şekilde bağlı azot bütün canlı cisimlerin, hayvan ve bitkisel hücrelerin iskelet maddesi olan proteinlerin esas kısımlarından biridir ve bunları teşkil eden amino asitlerini kimyasal bileşik halinde % 14 oranında azot bulunur. Vücuttaki azotun diğer bir kısmı purinlerde ve lesitinlerde, yine kimya olarak bağlı vaziyette bulunur.
Havanın atıl olan azotunu organizmalarındaki kimyasal bileşikler halinde tespit etmeğe ancak birkaç uzviyet sahip olduğundan ekseri bitkilerin gelişme imkanını artırmak için bunlara kimyasal şekilde bağlanmış azotu, sunî gübre olarak vermek lazımdır. Bu iş için hem amonyum tuzları hem de nitratlar elverişlidir. Bunların her ikisini de bitkiler kullanabilirler. Ancak tabiattaki azot çevrimi bir şekilde yapay azot bileşiklerinin kullanılmasından sonra bozulmuştur. Bunun sonucu olarak da akarsularda özellikle göllerde yosunlaşmaya sebep olan başlıca element azot ve azotif bileşiklerle algler aşırı büyümekte ve aşırı beslenme sonucu bataklaşma oluşmaktadır.
Hayvani hücreler ise azotu, bitkilerden aldıkları komplike bileşikler olan proteinler şeklinde kullanabilirler. Vücudumuz azot içeren proteinleri, üreye; kuşlar ve yerde sürünen hayvanlar ürik aside; fareler ise asit amide çevirirler.
Azot periyodik sistemde 5. grubun ilk elementidir. Normal şartlarda kimyasal bileşikler veya iki atomlu molekül haline de bulunur. Bu sebeple serbest atomu veya iyonları halinde bulunmaz. Bileşiklerinde azot atomları elektronlarını komşu atomlarla paylaşır, florür, oksijen ve klordan başka elementlerle yaptığı atomlardan alarak negatif yüklenir. Doğal sularda bulunduğu şekiller amonyak, nitrat iyonu, nitrit iyonudur.
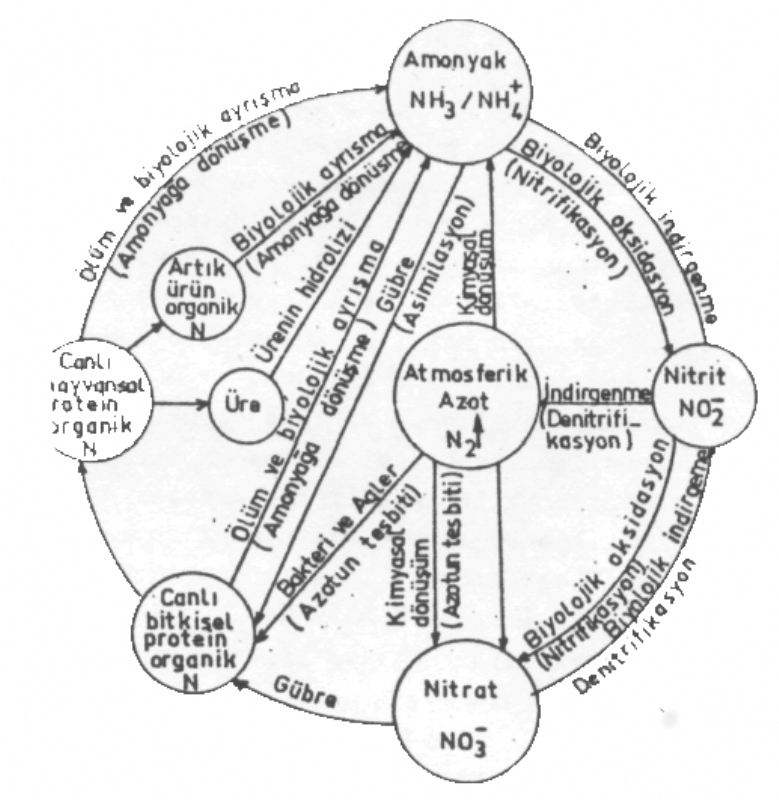
Tabiatta azot gazı, inorganik nitrit, nitrat ve amonyum iyonları ve protein gibi organik bileşikler arasında kimyasal değişimler olur ve azot devri meydana gelir.
Çevrimin azot deposunu atmosfer oluşturmaktadır. Canlı yaşamda önemli yaşamda önemli yeri olduğunu belirttiğimiz azot, doğadaki çeşitli evrelerden geçtikten sonra insana kadar ulaşmakta ve insan artıklarıyla çevreye dönerek devrini tamamlamaktadır. Doğada azot dolaşımı çok karmaşık bir biçimde süregeldiğinden, azot çevriminin su kaynaklarına uygulanarak göz önünde tutulması, bunların kontrolü açısından hangi süreçlerin önemli olduğu hakkında daha iyi bir fikir vermektedir.
Değişik şekilde su kaynaklarına verilen azot bileşikleri nedeni ile amonyağa dönüşme, nitrifikasyon, asimilasyon ve denitrifikasyon olayları meydana gelmektedir. Amonyağa dönüşme süre cinde organik azotun amonyağa dönüşümü mikroorganizmalar tarafından gerçekleştirilir. Bakteriler, ortamdaki amonyağı önce nitrite sonra nitrata oksitler. Bu olaya nitrifikasyon süreci denilir.
Oksidasyon işlemleri, mikroorganizmalar tarafından gerçekleştirilen biyokimyasal reaksiyonlar sonucu meydana geldiğinden, nitrifikasyon süreci inorganik azot bileşiklerinin biyokimyasal Oksidasyon olarak da tanımlanmaktadır.(Stratton 1966)
Biyokimyasal nitrifikasyon süreci başlıca 2 organizma gurubu tarafından gerçekleştirilir. "Nitrosomonas" denilen mikroorganizmalar, amonyağı nitrite dönüştürürken, "nitrobakter" denilen mikroorganizmalar da nitriti, nitrata oksitler. Her iki gruptaki mikroorganizmalar metabolizmaları için gerekli enerjiyi bu reaksiyonlardan sağlarlar. Bu mikroorganizmaların diğer bir özelliği de, hücre sentezleri için inorganik karbon kaynakları kullanmalarıdır.
Asimilasyonda ise nitrat bir taraftan bitkiler tarafından özümlenirken, bir taraftan da denitrifikasyon işlemi ile önce nitrit, sonra azot gazına dönüşerek atmosfere geri döner. Buna göre nitrifikasyon ve denitrifikasyon işlemleri, su kaynaklarında çözünmüş oksijen dengesini yansıtmaları açısından önem kazanır.
Akarsuların kirlenmesi açısından önemli olan, inorganik atık bileşiklerinin nitrifikasyon sürecindeki bünye değişimleriyle ortamdaki oksijen dengesinin bozulmasıdır. Nitrifikasyon sürecinde, enerji gereksinmelerini karşılamak için nitrosomonasların amonyağı nitrite ve nitrobakterlerin nitriti nitrata oksitlemeleri aşağıdaki reaksiyonlarla tanımlanır.
NH4+ + 1,5 O2 à 2H+ + H2O + NO2- (1)
NO2 - + 0,5 O2 à NO3- (2)
15 CO2 + 13NH4+ à 10 NO2- + 3C5H7NO2 + 23H+ + 4H2O (3)
Nitrosomonas
15 CO2 + NH4+ + 10 NO2- + 2H2O à 10NO3- + C5H7NO2 + H+ (4)
Nitrobakter
Bu bağıntılar nitrosomas ve nitrobakterlerin oksijen tüketimi ile dönüşüm oranlarının belirlenmesinde kullanılmaktadır.
Buna göre nitrosomonas ve nitrobakter için dönüşüm oranları, 0,15 mg / hücre / mg NH4+-N ve 0,02 mg hücre / mg NO2--N değerlerini almaktadır. Oysa bu oranlar, termodinamik teoriden yararlanarak 0,29 mg hücre / mg NH4+-N , 0,084 mg hücre / mg NO2--N olarak elde edilmiştir. Buna dayanılarak,120 mg / lt amonyak azotunun harcanmasına karşılık sadece 1,8 mg / lt toplam bakterinin oluşacağı söylenebilir.(1) ve (2) bağıntılarına göre, 1 mg amonyak azotunun nitrite oksidasyonu için 3,43 mg O2 ve 1 mg nitritin nitrata oksidasyonu içinde 1,14 mg O2 gereksinmesine rağmen, nitrifikasyon mekanizması ile ilgili araştırmalarda bu değerlerin 3,22 mg O2 / mg NH4+-N ve 1,11 mg O2 / mg NO2--N olduğu gösterilmiştir. Ancak pratikteki uygulamalarda, toplam olarak 1 mg inorganik azotun oksidasyonu için, oksijen gereksinmesinin 4,6 değerinde olması yeterli bir yaklaşımdır. Buna göre nitrifikasyon için gerekli oksijen miktarı, 30 mg / lt amonyak azotunun oksidasyonu için 138 mg / lt gibi önemli bir değere yükselmektedir. Azotlu maddelerle kirletilmiş bu tür bir akarsuda oksijen gereksinmesi, akarsu bünyesindeki çözünmüş oksijenle karşılandığından, ortamdaki oksijen dengesi bozulmaktadır.
Atmosferde azot başlıca azot molekülü halindedir, fakat az miktarda amonyak, azot oksitleri gibi çeşitli bileşikleri de bulunur. Atmosferik NH3 hava kirlenmesinden, hayvan ve bitki artıklarının bozunmasından, topraktan ve stratosferdeki başlıca fotokimyasal reaksiyonlardan ve havada en yaygın bulunan N2O4 fırtınalı havalardaki elektriksel enerjiden, yakma ile hava kirlenmesinden meydana gelir. Yağmur suyu, aşağı inerken havadaki amonyağı ve azot oksitlerini alır. Atmosferik azotun önemli bir kısmı kimyasal yollarla sentetik olarak amonyağa ve sonra da nitrata çevrilerek gübre yapılmaktadır.
Yeryüzündeki azotun çoğu gaz halinde ve organik azot şeklindedir. Bunun da başlıca kısmı çözünmez haldedir ve tabiatta hayat başladıktan beri uzun seneler içinde birikim yapmıştır. Yüzey sularında inorganik azot bileşikleri genellikle bir kaç mg / lt konsantrasyonu geçmez, fakat yeraltı sularında 100 mg / lt ye kadar bulunabilir, düşük konsantrasyonlarda bile sularda yaşayan bitkilerin gelişmesini kolaylaştırır.
Ev atıklarında, moleküler azot hariç, toplam azot konsantrasyonu 18 - 28 mg / lt arasında değişir. Bunun bir kısmı bileşikler halindedir. Tarımsal drenaj sularında azot konsantrasyonu genelde 1 - 100 mg / lt arasında değişir ve çoğu nitrat halindedir. Çok fazla sediment içeren akışlarda çok miktarda azot partikülleri ve bunlara adsorplanmış halde amonyak azotu vardır. Yeraltı suları topraktan geçerken amonyağın oksitlenmesiyle meydana gelen nitratları çözer. Göllerde en çok organik azot ve ondan sonra nitrat azotu bulunur. Bilhassa yazın fotosentezle organizmalar inorganik azotu, organiğe çevirirler ve aynı zamanda nitrifikasyon da yazın daha kolay tamamlandığı için nitrat miktarı artar.
Sorhocam.com 2014 yılında Ziraat Mühendisi Arafa KARAÇELEBİ tarafından kurulmuş olup herkesin faydalanabilmesi için ücretsiz olarak hizmet vermektedir.
Bitki hastalıkları, bitki zararlıları, yabancı otlar, şifalı bitkiler, arıcılık, bayilik sınavı notları, bayilik sınavı soruları, online testler, kimyasal analiz yöntemleri, bitki besleme ve gübreleme, tarımsal destekler, peysaj ve süs bitkileri, kimyasal analiz yöntemleri, hijyen eğitimi, pest kontrol yöntemleri


